Изучения взаимодействия белков поможет создать лекарства против муковисцидоза
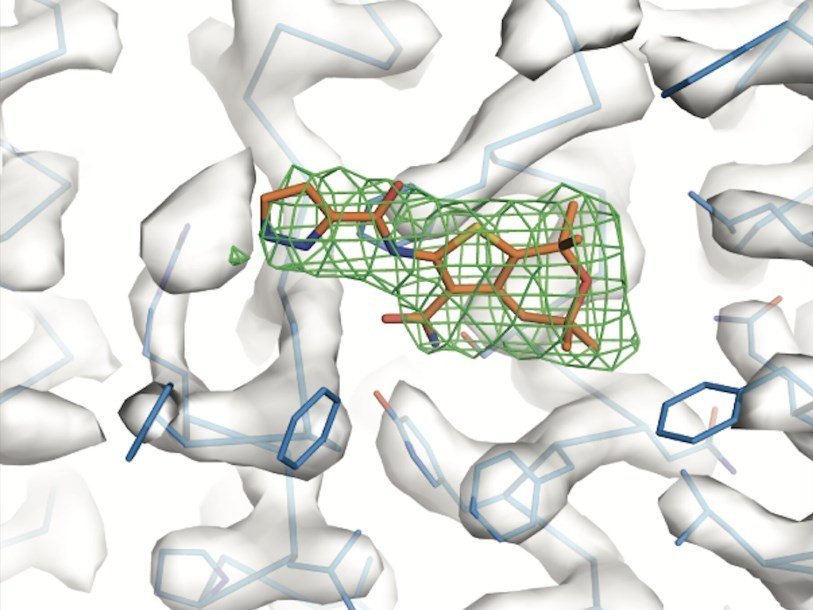
Учёные из Рокфеллеровского университета, Калифорнийского университета в Сан-Франциско и Медицинского института имени Говарда Хьюза изучили на атомном уровне работу существующих лекарств против муковисцидоза. Детали взаимодействия препаратов с клеточным белком помогут в разработке новых, более эффективных средств лечения этой болезни.
При муковисцидозе из-за мутации в одном из генов нарушается структура и работа трансмембранного регулятора проводимости (CFTR) – белка, служащего для перемещения ионов хлора через клеточную мембрану. Проявляется болезнь в виде изменений в составе слизистой оболочки внутренних органов. Слизь становится более густой, особенно опасно это в лёгких, так как из-за густой, плохо отделяемой слизи там часто возникают инфекции, в дальнейшем развитие болезни ведёт к дыхательной недостаточности. Врачи пока могут предоставить больным муковисцидозом лишь симптоматическое лечение. Также разрабатываются методы генной терапии этого заболевания. В 2010-х годах при муковисцидозе стали применять пересадку донорских лёгких.
Недавно появились новые препараты, которые называют потенциаторами. Это вещества, вступающие в реакцию с дефектным CFTR и улучшающие его функции. В настоящее время на рынке имеется только один такой препарат — ивакафтор; другой, GLPG1837, пока проходит испытания. Ивакафтор улучшает работу лёгких при муковисцидозе примерно на 10%, и не для каждого больного он оказывается эффективным. Поэтому врачи хотели бы создать новые, более действенные потенциаторы.
Авторы исследования использовали криоэлектронную микроскопию, чтобы проследить взаимодействие ивакафтора и GLPG1837 с белком CFTR. Данный метод позволяет получить детальные изображения пространственной структуры взаимодействующих белков (подробнее о криоэлектронной микроскопии можно узнать в очерке «Разглядеть замороженные молекулы»). Оказалось, что оба потенциатора присоединяются к CFTR на одном и том же участке молекулы. Руководитель исследования профессор Цзюэ Чень (Jue Chen) сравнивает этот участок с шарниром, который то открывает, то закрывает проход в мембране. При соединении с потенциаторами шарнир застывает в открытом состоянии, что облегчает переход ионов через клеточную мембрану и, в итоге, симптомы болезни.
Зная структуру этого ключевого участка молекулы, учёные смогут смоделировать, а затем синтезировать новые препараты, молекулы которых будут более действенно связываться с CFTR и открывать трансмембранный канал.
Цзюэ Чень и её коллеги открыто опубликовали полученные данные, чтобы ими могли воспользоваться все исследователи, работающие над лекарствами от муковисцидоза. Как сказала Цзюэ Чень, появление нескольких препаратов создаст необходимую конкуренцию и снизит стоимость лечения, сделав его доступнее для больных.
Исследование опубликовано в журнале Science.







Комментарии